2025/08/19
ニトロソアミンとは?
ニトロソアミンは、タバコの煙に含まれる主要な変異原性物質である。ニトロソアミンは亜硝酸塩に食品中のアミンが結合して生成するので、亜硝酸塩を含む食品が問題となる。例えば、ハムやソーセージには、微生物による腐敗を防止し、さらに肉を赤色に保つために、現在でも亜硝酸塩が使用されている。また、葉野菜には、肥料成分である硝酸塩が残留硝酸塩として、一定量含まれているが、そのような野菜を食べると、口の中の微生物により硝酸塩が亜硝酸塩に還元され、その亜硝酸塩が胃の酸性条件下でアミンと反応
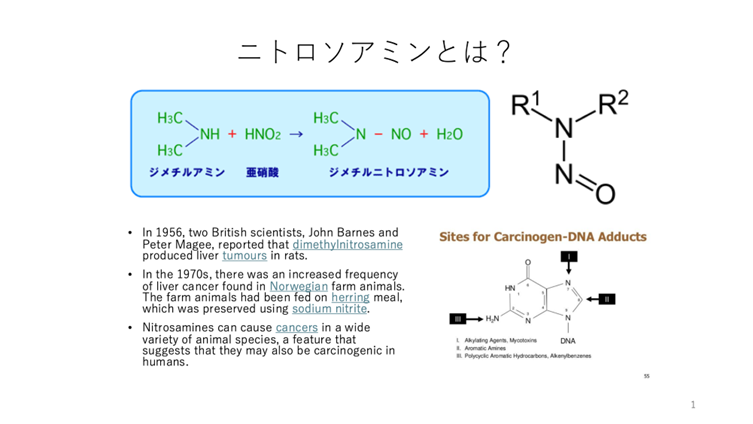
するとニトロソアミンが生成する。そのニトロソアミンが消化器系の発がんに関係することが指摘されてきた。
このブログでは、大部分のがんは、慢性炎症で発生する活性酸素種が遺伝子を変異させることにより、生成すると述べてきた。このニトロソアミンなど環境化学物質による遺伝子変異は、がん化にどの程度寄与すると考えられるのか。もちろん、高濃度のニトロソアミンを長期間体内に入れれば、その害により遺伝子変異が蓄積して、細胞ががん化することは当然考えられる。問題はそのような具体例があるかどうかである。
体内に入ったニトロソアミンは、肝臓などで代謝され、DNAを攻撃する「アルキル化剤」という物質に変化する。このアルキル化剤は、DNAの4つの塩基のうち、特にグアニン(G)に結合して、これを傷つける。DNAが複製される際、この傷ついたグアニンは、本来のパートナーであるシトシン(C)ではなく、誤ってチミン(T)とペアを組んでしまいます。この「ペアミス」が起きたまま細胞分裂が進むと、元の「G」だった塩基が最終的に「A(アデニン)」に置き換わってしまいます。これがニトロソアミンに特徴的なG→A(G:C→A:T)点突然変異である。このG→A変異は、ヒトのがん細胞から実際に見つかっており、ニトロソアミン曝露との強い関連を示している、と指摘されている。
喫煙者の肺がん組織では、がんの増殖に直接関わるKRAS遺伝子や、がんを抑制するTP53遺伝子に、特徴的なG→A変異が高い頻度で見つかっている。食道がん・膵臓がん: これらの喫煙と関連の深いがんでも、同様のメカニズムが関与していると考えられている。
加工肉(ベーコン、ハムなど)に含まれる亜硝酸塩や、一部の保存食に含まれる亜硝酸塩は、胃の中でアミン類と反応してニトロソアミンを生成することがある。食道がん・胃がん: これらの食品の摂取量が多い地域では、食道がんや胃がんの発生率が高いことが知られている。そして、それらの地域のがん患者の組織から、がん抑制遺伝子であるTP53遺伝子にG→A変異が多く見つかることが報告されており、食事由来のニトロソアミンががんのリスク因子であることが強く示唆されている。
ニトロソアミンの作用は抗酸化成分によって抑制される
抗酸化成分は、ニトロソアミンによる発がんリスクを複数の段階でブロックするように働く。特に重要なのは、ニトロソアミンが「生成される前」と「体内でダメージを与える際」の両方に関与することである。抗酸化成分が発がんを抑制する主なメカニズムとしては、次の二つが考えられる。
1)ニトロソアミンの「生成そのもの」を阻害する
これが最も直接的で重要なメカニズムである。胃の中など酸性の環境では、食品に含まれる「亜硝酸」と「アミン類」が反応してニトロソアミンが生成される。ビタミンC(アスコルビン酸)は、アミン類よりも先に亜硝酸と素早く反応する。いわば、亜硝酸のパートナーを「横取り」するような形で、亜硝酸を無害な一酸化窒素(NO)に変化させます。その結果、発がん性のあるニトロソアミンが作られること自体を防ぐことができる。例えば、加工肉(亜硝酸を含む)と一緒にビタミンCが豊富な野菜や果物を食べると、胃の中でのニトロソアミン生成が抑制されることが知られている。
2)体内での「酸化的ダメージ」を軽減する
ニトロソアミンが体内で代謝される過程や、それが引き起こす炎症反応では、遺伝子を傷つける「活性酸素(ROS)」も同時に発生する。ビタミンEや、お茶に含まれるカテキンなどのポリフェノール類は、強力な抗酸化作用を持つ。これらの成分が活性酸素を消去することで、ニトロソアミンによる直接的なDNA損傷(アルキル化)に加えて、活性酸素による間接的なDNA損傷も軽減します。これにより、遺伝子変異のリスクを二重に抑える効果が期待できる。具体的な成分と研究例として、
* ビタミンC: ニトロソアミン生成阻害の主役
疫学研究では、ビタミンCを多く含む野菜や果物の摂取が、胃がんなどのリスクを下げると報告されている。
* ビタミンE: 脂溶性の抗酸化物質で、細胞膜などを酸化ダメージから守る。
* カテキン(緑茶): 緑茶に含まれるカテキン(特にEGCG)は、ニトロソアミンの生成を抑制する作用と、高い抗酸化作用の両方を持ち合わせる。緑茶をよく飲む習慣のある地域で、胃がんや食道がんの発生率が低いことを示す研究もある。
結論として、抗酸化成分、特にビタミンCを豊富に含む食事は、ニトロソアミンの生成を効果的に抑制し、発がんリスクを低減させるための合理的な生活習慣と言える。
このように、ニトロソアミンは遺伝子を変異させ、発がん性が指摘されるが、問題はニトロソアミンがどれだけの濃度で、どの程度の期間作用するかである。国立がん研究センターと理研の共同研究により、肝臓がん細胞の全塩基配列を300例について解析した結果によると、細胞あたり約1万箇所の点突然変異があった、とのことである。一つの細胞あたり1万カ所の変異を引き起こすニトロソアミンの摂取量は、どのくらいになるのか。しかも、ニトロソアミンが少量ずつ細胞に作用した場合、DNA修復系によりその変異は取り除かれてしまう。変異が蓄積するためには、一定濃度以上のニトロソアミンが連続的に作用する必要がある。タバコを一日に何箱分も吸い続けると、その1万箇所に到達するのか、現在それを判断できるデータはない。
野菜の場合はどうか。国のデータによっても、5000 ppm を超える硝酸塩を含む野菜は多い。これを毎日食べたとして、どの程度のニトロソアミンの生成になるのか。農水省によると、口の中の微生物により、食べた野菜に含まれる硝酸塩の約5%が、亜硝酸に変換されるという。とろころが、上述のように、野菜に含まれる抗酸化成分は、胃の中のニトロソアミンの生成を阻害する。量的な推論は困難であるが、野菜を食べたことによるニトロソアミンの生成は、抗酸化成分の効果で相殺される可能性もある。いずれにしても、ニトロソアミンによる実際の発がんの程度を推定するデータは、現在のところない。
ニトロソアミンか活性酸素か、という問題をさらに複雑にしているのは、ニトロソアミンが炎症を引き起こすことである。ニトロソアミンが体内の酵素(特にCYP2E1)によって代謝される際、その副産物として大量の活性酸素(ROS)が発生する。発生した活性酸素は、細胞の膜、タンパク質、そしてDNAなどを無差別に攻撃し、酸化させて傷つける。この状態が「酸化ストレス」である。
細胞が酸化ストレスによって傷つけられると、体はそれを「異常事態」とみなし、修復しようとする。この防御反応のスイッチとして、炎症性サイトカイン(TNF-αやIL-6など)と呼ばれる物質が放出され、免疫細胞(マクロファージなど)が患部に集まってくる。これが「炎症」の始まりである。 集まってきた免疫細胞は、異物を排除するために自らも活性酸素を放出する。これにより、酸化ストレスがさらに悪化する。慢性的な炎症は、傷ついた組織を修復しようと細胞分裂を促する。しかし、この環境下ではDNAに傷がついた異常な細胞が増殖しやすくなり、がん化のリスクが著しく高まる。
つまり、ニトロソアミンは、①直接的なDNA損傷(遺伝子変異の誘発)、②酸化ストレスを介した慢性炎症の誘発という2つのルートで、がんの発生と進行を強力に後押しする。炎症は、がん細胞が育ちやすい「土壌」を作ってしまう、と考えることもできる。
結論として、1日に何箱ものタバコを吸うヘビースモーカーの場合には、ニトロソアミンのみで肺がんなどを起こす可能性があるかもしれない。ただし、野菜に含まれる残留硝酸塩による発がんが、過去には心配されたが、抗酸化成分による相殺効果を考えれば、それほど心配する必要はないのかもしれない。特に、残留硝酸塩を通常の1/5〜1/10程度に下げた e健康野菜(e野菜)は、抗酸化成分が通常の数倍〜10数倍多いので、健康には非常に良いことになる。また、ニトロソアミンが炎症を引き起こすことを見れば、ニトロソアミンの害は、活性酸素の害に置き換わるので、「大部分のがんでは、慢性炎症による活性酸素が遺伝子変異の主な要因である」ことは、現時点では変更する理由がない、と考えられる。